\[ \Delta d = \alpha \cdot d_0 \cdot \Delta T \] Donde:
- \(\Delta d\) — cambio en la longitud (en metros, \(m\))
- \(\alpha\) — coeficiente de expansión térmica lineal(en \(°C^{-1}\))
- \(d_0\) — longitud inicial (en metros, \(m\))
- \(\Delta T\) — cambio en la temperatura (en grados Celsius, \(°C\))
\[ \Delta V_1 = \beta \cdot V_0 \cdot \Delta T \] Donde:
- \(\Delta V\) — cambio en el volumen (en metros cúbicos, \(m^3\))
- \(\beta\) — coeficiente de expansión térmica volumétrica (en \(°C^{-1}\))
- \(V_0\) — volumen inicial (en metros cúbicos, \(m^3\))
- \(\Delta T\) — cambio en la temperatura (en grados Celsius, \(°C\))
\[ Q = m \cdot c \cdot \Delta T \] Donde:
- \(Q\) — cantidad de calor (en joules, \(J\))
- \(m\) — masa del cuerpo (en kilogramos, \(kg\))
-
\(c\) — calor específico del material
Puede estar en:- \(cal/(g\cdot°C)\)
- \(cal/(g\cdot K)\)
- \(J/(kg\cdot°C)\)
- \(J/(kg\cdot K)\)
- \(\Delta T\) — variación de temperatura (en \(°C\))
\[ P \color{gray} [W] \color{black} = \frac{Q \color{gray} [J] \color{black}}{t \color{gray} [s] \color{black}} \] Donde:
- \(P\) — potencia (en watts, \(W\) o \(J/s\))
- \(Q\) — cantidad de calor (en joules, \(J\))
- \(t\) — tiempo (en segundos, \(s\))
Despejes:
- \(V\): Volumen del gas (en metros cúbicos, \(m^3\))
- \(p\): Presión absoluta (en pascales, \(Pa\))
- \(n\): Número de moles del gas (en moles, \(mol\))
- \(R\): Constante universal de los gases \[ R \approx 8{,}314 \, \frac{J}{mol \cdot K} \]
- \(T\): Temperatura del gas (en kelvin, \(K\))
08- Física II Práctico TP3 - Parte A - Gases ideales - Ecuación de Estado 2021
Presión constante \(p = \text{constante}\) \[ W = \int_{V_1}^{V_2} p dV \] Aplicando la integral \[ W = p(V_2 - V_1) \quad \text{ o } \quad W = nR(T_2 - T_1) \]
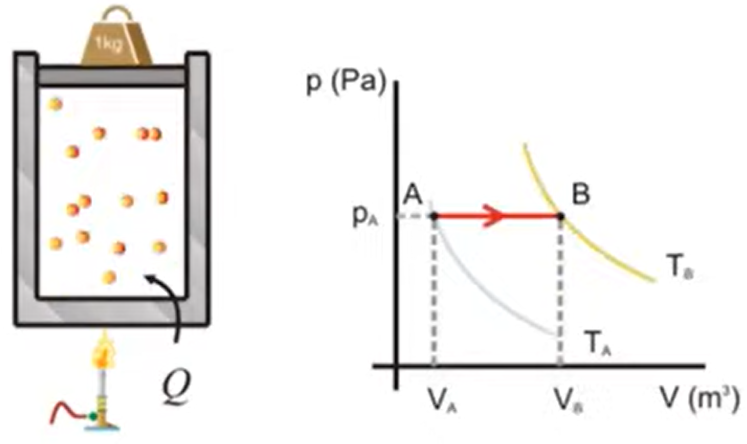
- \(W\): Trabajo (en joules, \(J\))
- \(p\): Presión (en pascales, \(Pa\))
- \(V_1\): Volumen inicial (en metros cúbicos, \(m^3\))
- \(V_2\): Volumen final (en metros cúbicos, \(m^3\))
- \(n\): Número de moles del gas (en moles, \(mol\))
- \(R\): Constante universal de los gases \[ R \approx 8{,}314 \, \frac{J}{mol \cdot K} \]
09- Física II Práctico TP3 - Parte B - Transformaciones en Gases Ideales 2021
Tempratura constante \(T = \text{constante}\) \[ W = nRT \int_{V_1}^{V_2} \frac{1}{V} dV \] Aplicando la integral \[ W = nRT \ln \left( \frac{V_2}{V_1} \right) \quad \text{ o } \quad W = nRT \ln \left( \frac{T_2}{T_1} \right) \]
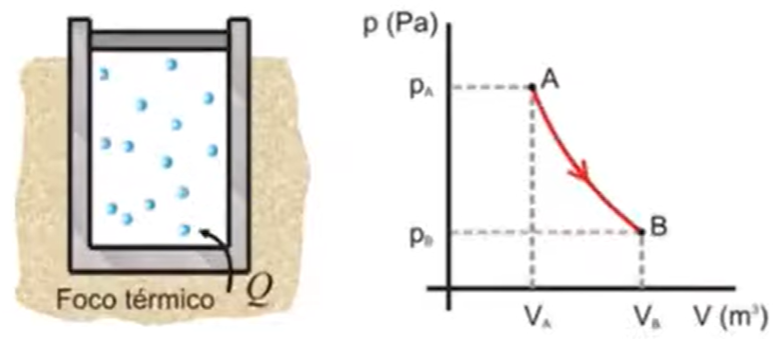
- \(W\): Trabajo (en joules, \(J\))
- \(n\): Número de moles del gas (en moles, \(mol\))
- \(R\): Constante universal de los gases \[ R \approx 8{,}314 \, \frac{J}{mol \cdot K} \]
- \(T\): Temperatura del gas (en kelvin, \(K\))
- \(V_1\): Volumen inicial (en metros cúbicos, \(m^3\))
- \(V_2\): Volumen final (en metros cúbicos, \(m^3\))
No entra ni sale calor del sistema \[ W = \int_{V_1}^{V_2} p dV \] Resolviendo la integral \[ W = \frac{p_1 V_1 - p_2 V_2}{\gamma - 1} \]
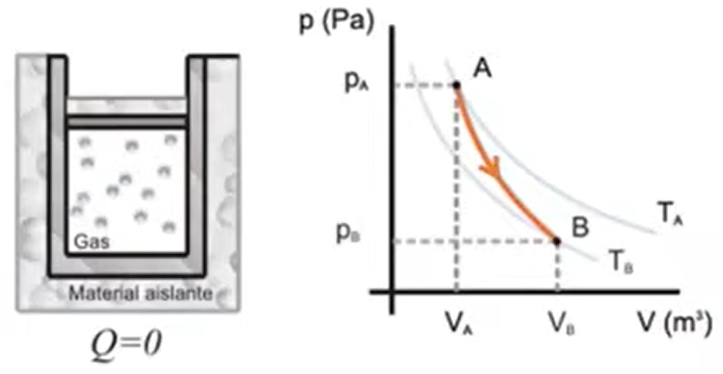
- \(W\): Trabajo (en joules, \(J\))
- \(p_1\): Presión inicial (en pascales, \(Pa\))
- \(p_2\): Presión final (en pascales, \(Pa\))
- \(V_1\): Volumen inicial (en metros cúbicos, \(m^3\))
- \(V_2\): Volumen final (en metros cúbicos, \(m^3\))
- \(\gamma\): Coeficiente adiabático (adimensional) \[ \gamma = \tfrac{5}{3} \approx 1{,}67 \quad \text{(gas monoatómico)} \] \[ \gamma = \tfrac{7}{5} = 1{,}4 \quad \text{(gas diatómico, ej. aire)} \]
Volumen constante \(V = \text{constante}\) \[ W = \int_{V_1}^{V_2} p dV \] Debido a que no hay cambio de volumen, obtenemos: \[ W = 0 \]
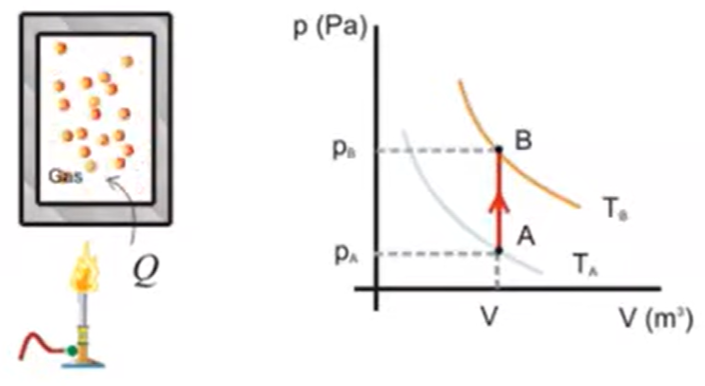
- \(\Delta U\): Cambio de energía interna (en joules, \(J\))
- \(Q\): Calor (en joules, \(J\))
- \(W\): Trabajo (en joules, \(J\))
10- Física II Práctico TP4 - 1er Principio de la Termodinámica 2021
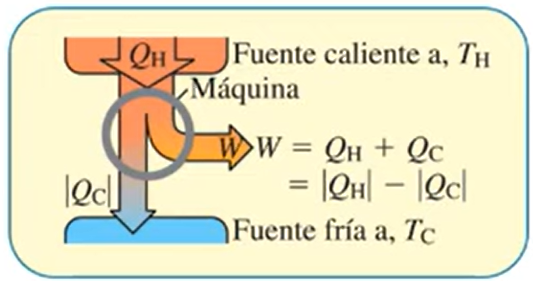
- \(e\): Eficiencia de la máquina térmica (adimensional)
- \(W\): Trabajo realizado por la máquina térmica (en joules, \(J\))
- \(Q_H\): Calor absorbido por la máquina térmica (en joules, \(J\))
- \(Q_C\): Calor cedido por la máquina térmica (en joules, \(J\))
11- Física II Práctico TP5 - 2do Principio de la Termodinámica, Ciclo Carnot 2021
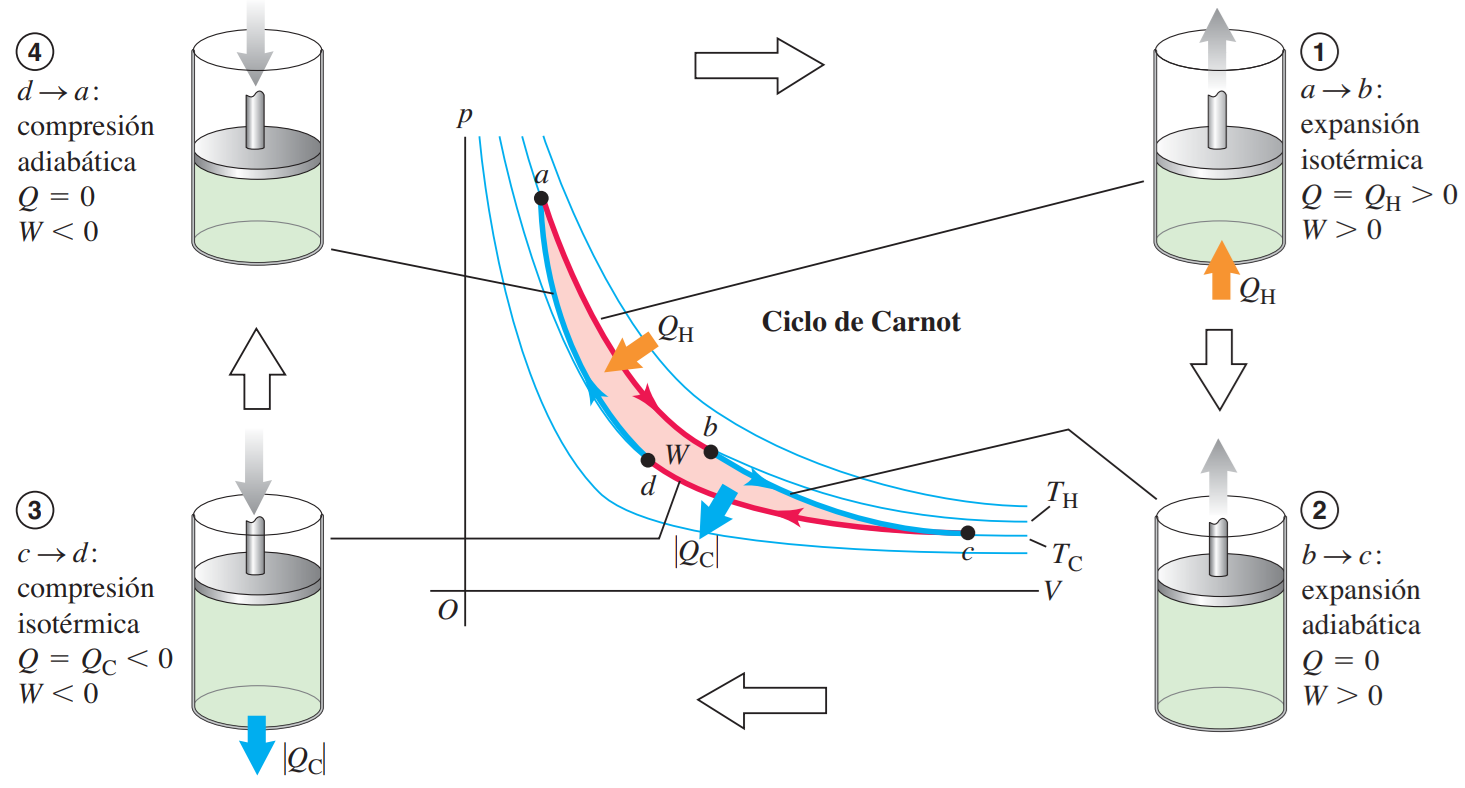
- \(e_{\text{carnot}}\): Eficiencia de la máquina térmica de Carnot (adimensional)
- \(T_H\): Temperatura absoluta de la fuente caliente (en kelvin, \(K\))
- \(T_C\): Temperatura absoluta de la fuente fría (en kelvin, \(K\))
11- Física II Práctico TP5 - 2do Principio de la Termodinámica, Ciclo Carnot 2021
Balance energético del refrigerador: \[ |Q_H| = |Q_C| + |W| \] Eficiencia: \[ K = \frac{|Q_C|}{|W|} = \frac{|Q_C|}{|Q_H| - |Q_C|} \]
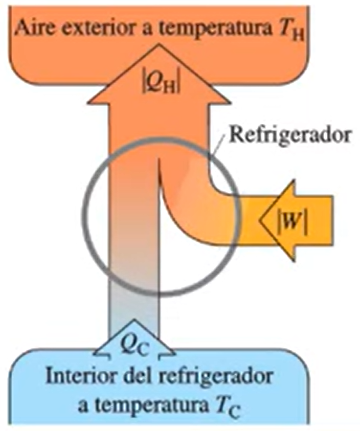
- \(K\): Coeficiente de rendimiento de un refrigerador
- \(|Q_H|\): Calor absorbido por el refrigerador (en joules, \(J\))
- \(|Q_C|\): Calor cedido por el refrigerador (en joules, \(J\))
- \(|W|\): Trabajo realizado por el refrigerador (en joules, \(J\))
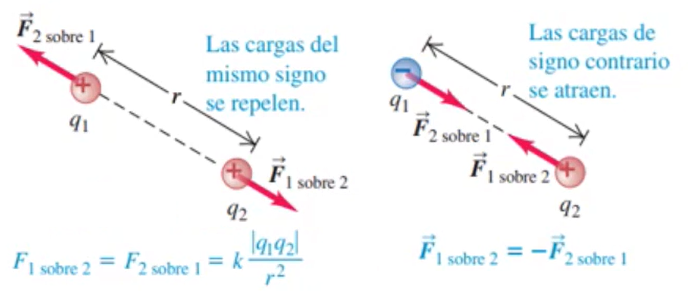
- \(F\): Fuerza eléctrica (en newtons, \(N\))
-
\(k\): Constante de Coulomb (en newtons, \(N\))
\[ k \approx 9 \times 10^9 \frac{N m^2}{C^2} \] - \(q_1\): Carga eléctrica (en coulombs, \(C\))
- \(q_2\): Carga eléctrica (en coulombs, \(C\))
- \(r\): Distancia entre las cargas (en metros, \(m\))
Celsius ↔ Fahrenheit: \[ T_{°F} = \frac{9}{5} \cdot T_{°C} + 32 \] \[ T_{°C} = \frac{5}{9} \cdot (T_{°F} - 32) \] Celsius ↔ Kelvin: \[ T_K = T_{°C} + 273{,}15 \] \[ T_{°C} = T_K - 273{,}15 \] Salto térmico (variación): \[ \Delta T_{°F} = \frac{9}{5} \cdot \Delta T_{°C} \] \[ \Delta T_{°C} = \Delta T_K \]
\[ Q = m \cdot L \] Donde:
- \(Q\) — cantidad de calor (en joules, \(J\))
- \(m\) — masa del cuerpo (en kilogramos, \(kg\))
- \(L\) — calor latente del material (en \(J/kg\))
\(L > 0\) si el proceso absorbe calor (fusión, vaporización); \(L < 0\) si lo cede (solidificación, condensación).
Volumen constante \(V = \text{constante}\) \[ \frac{P}{T} = \text{constante} \quad \Rightarrow \quad \frac{P_1}{T_1} = \frac{P_2}{T_2} \] Donde:
- \(P_1\) — presión inicial (en pascales, \(Pa\))
- \(P_2\) — presión final (en pascales, \(Pa\))
- \(T_1\) — temperatura inicial (en kelvin, \(K\))
- \(T_2\) — temperatura final (en kelvin, \(K\))
Coeficiente volumétrico de un recipiente sólido isotrópico: \[ \gamma_{\text{recipiente}} = 3\alpha \] Donde:
- \(\gamma_{\text{recipiente}}\) — coeficiente de expansión volumétrica del recipiente (en \(°C^{-1}\))
- \(\alpha\) — coeficiente de expansión lineal del sólido (en \(°C^{-1}\))
Válido para sólidos isotrópicos con variaciones de temperatura pequeñas.
¿Qué es un sólido isotrópico?
Joule en unidades base del SI: \[ J = N \cdot m = \frac{kg \cdot m^2}{s^2} \] Calorías ↔ Joules: \[ 1 \, \text{cal} = 4{,}186 \, J \] \[ 1 \, J \approx 0{,}239 \, \text{cal} \] Calor específico — \(\text{cal}/(g \cdot °C)\) ↔ \(J/(kg \cdot °C)\): \[ \frac{\text{cal}}{g \cdot °C} \;\xrightarrow{\times\,4186}\; \frac{J}{kg \cdot °C} \] \[ \frac{J}{kg \cdot °C} \;\xrightarrow{\div\,4186}\; \frac{\text{cal}}{g \cdot °C} \] \(J/(kg \cdot K)\) vs \(J/(kg \cdot °C)\): son equivalentes, ya que \(\Delta T_K = \Delta T_{°C}\).
Pascales ↔ Atmósferas: \[ 1 \, \text{atm} = 101\,325 \, Pa \approx 1{,}013 \times 10^5 \, Pa \] \[ 1 \, Pa \approx 9{,}87 \times 10^{-6} \, \text{atm} \]
Litros ↔ Metros cúbicos: \[ 1 \, L = 10^{-3} \, m^3 = 0{,}001 \, m^3 \] \[ 1 \, m^3 = 1000 \, L \]
Volumen de un gas ideal (despejado de \(pV = nRT\)): \[ V = \frac{n R T}{p} \] Donde:
- \(V\) — volumen del gas (en metros cúbicos, \(m^3\), o en litros si se usa \(R = 0{,}082 \, \frac{L \cdot atm}{mol \cdot K}\))
- \(n\) — número de moles (en moles, \(mol\))
- \(R\) — constante universal de los gases: \[ R \approx 8{,}314 \, \frac{J}{mol \cdot K} \quad \text{o} \quad R \approx 0{,}082 \, \frac{L \cdot atm}{mol \cdot K} \]
- \(T\) — temperatura (en kelvin, \(K\))
- \(p\) — presión (en pascales, \(Pa\), o en atmósferas si se usa \(R\) en \(L \cdot atm\))
Variación de entropía a temperatura constante: \[ \Delta S = \frac{Q}{T} \] Donde:
- \(\Delta S\) — variación de entropía (en \(J/K\) o \(cal/K\))
- \(Q\) — calor intercambiado (en joules, \(J\), o en calorías, \(cal\))
- \(T\) — temperatura absoluta del proceso (en kelvin, \(K\))
Válido únicamente para procesos isotérmicos (temperatura constante). Si \(Q > 0\) (calor absorbido), \(\Delta S > 0\) (entropía aumenta).
Cuando la trayectoria en el diagrama pV sigue una línea recta oblicua (ni p ni V
constantes), se obtiene la ecuación de la recta y se integra:
1. Pendiente de la recta:
\[
m = \frac{P_2 - P_1}{V_2 - V_1} \color{gray}\left[\frac{\text{kPa}}{\text{m}^3}\right]\color{black}
\]
2. Presión como función del volumen:
\[
p(V) = P_1 + m(V - V_1)
\]
3. Trabajo:
\[
W = \int_{V_1}^{V_2} p(V)\,dV \color{gray}[\text{kJ}]\color{black}
\]
Donde:
- \(p(V)\) — presión como función del volumen, siguiendo la ecuación de la recta en el diagrama pV (en kPa)
- \(V_1, V_2\) — volumen inicial y final (en m³)
- \(P_1, P_2\) — presión inicial y final (en kPa)
- \(m\) — pendiente de la recta en el diagrama pV (en kPa/m³)
- \(W\) — trabajo (en kJ si p en kPa y V en m³)
\[
E = k \frac{|Q|}{r^2}
\]
Origen (sustituyendo la Ley de Coulomb en la definición de campo):
\[
\vec{E} = \frac{\vec{F}}{q_0}
= \frac{k\,\dfrac{|Q|\,q_0}{r^2}}{q_0}
= k \frac{|Q|}{r^2}
\]
La definición parte de vectores (\(\vec{E}\), \(\vec{F}\)), pero la fórmula resultante
\(E = k|Q|/r^2\) da la magnitud (escalar): el valor absoluto
en el numerador ya elimina el signo. La dirección se determina aparte
según si \(Q\) atrae o repele a \(q_0\).
La \(q_0\) (carga de prueba imaginaria positiva) se cancela: el campo es una propiedad del espacio, independiente de \(q_0\).
Donde:
- \(E\) — magnitud del campo eléctrico (en \(N/C\))
- \(k \approx 9 \times 10^9\;\dfrac{N \cdot m^2}{C^2}\) — constante de Coulomb
- \(Q\) — carga que genera el campo (en coulombs, \(C\))
- \(r\) — distancia desde \(Q\) hasta el punto (en metros, \(m\))
- \(q_0\) — carga de prueba positiva imaginaria (se cancela)
Deducción: al detenerse el objeto, toda su energía cinética se convierte en energía interna (calor). Como el sistema es adiabático, no hay pérdidas al exterior, entonces: \[ \underbrace{\Delta K}_{\text{variación de energía cinética}} = \underbrace{Q}_{\text{calor absorbido por el objeto}} \] \[ \frac{1}{2} m v^2 = m \, c \, \Delta T \] La masa \(m\) aparece en ambos miembros y se cancela: \[ \frac{1}{2} v^2 = c \, \Delta T \] Despejando \(\Delta T\): \[ \Delta T = \frac{v^2}{2 \, c} \] Donde:
- \(\Delta T\) — elevación de temperatura (en \(°C\))
- \(v\) — velocidad inicial del objeto (en \(m/s\))
- \(c\) — calor específico del material (en \(J/(kg \cdot °C)\))
El resultado es independiente de la masa del objeto.
Atención con las unidades: esta fórmula simplificada es válida únicamente con \(v\) en \(\text{m/s}\) y \(c\) en \(\text{J/(kg·°C)}\). Si el dato de \(c\) está en otras unidades (p. ej. \(\text{cal/(g·°C)}\)), no se puede sustituir directamente. En ese caso, calcular primero la energía cinética y luego despejar \(\Delta T\): \[ E_k = \tfrac{1}{2} m v^2 \quad [J] \] \[ \Delta T = \frac{E_k}{m \cdot c} \] asegurándose de que \(E_k\), \(m\) y \(c\) estén en unidades coherentes (p. ej. convertir \(E_k\) de J a cal usando \(1\,\text{cal} = 4{,}186\,J\) antes de dividir por \(c\) en cal/(g·°C)).
Relación esfuerzo-deformación (Ley de Hooke generalizada): \[ \frac{F}{S} = Y \cdot \frac{\Delta L}{L_0} \] Despejando \(F\): \[ F = Y \cdot S \cdot \frac{\Delta L}{L_0} \] Donde:
- \(F\) — fuerza aplicada (en newtons, \(N\))
- \(S\) — sección transversal del material (en \(m^2\))
- \(Y\) — módulo de Young o módulo de elasticidad (en pascales, \(Pa\))
- \(\Delta L\) — cambio de longitud (en metros, \(m\))
- \(L_0\) — longitud original (en metros, \(m\))
\(F/S\) es el esfuerzo (tensión mecánica, en \(Pa\)). \(\Delta L / L_0\) es la deformación unitaria (adimensional).
Deducción: para impedir el alargamiento, la fuerza de compresión debe compensar exactamente la dilatación térmica \(\Delta L = L_0 \cdot \alpha \cdot \Delta T\). Sustituyendo en \(F = Y \cdot S \cdot \Delta L / L_0\), el \(L_0\) se cancela: \[ F = Y \cdot S \cdot \alpha \cdot \Delta T \] Donde:
- \(F\) — fuerza de compresión necesaria (en newtons, \(N\))
- \(Y\) — módulo de Young del material (en pascales, \(Pa\))
- \(S\) — sección transversal (en \(m^2\))
- \(\alpha\) — coeficiente de expansión lineal (en \(°C^{-1}\))
- \(\Delta T\) — variación de temperatura (en \(°C\) o \(K\))
Atención con las unidades: \(Y\) suele darse en \(GPa\); convertir a \(Pa\) antes de operar (\(1\,GPa = 10^9\,Pa\)). La sección transversal debe estar en \(m^2\) (\(1\,cm^2 = 10^{-4}\,m^2\)).
Ejercicio 53 — ejemplo de aplicación